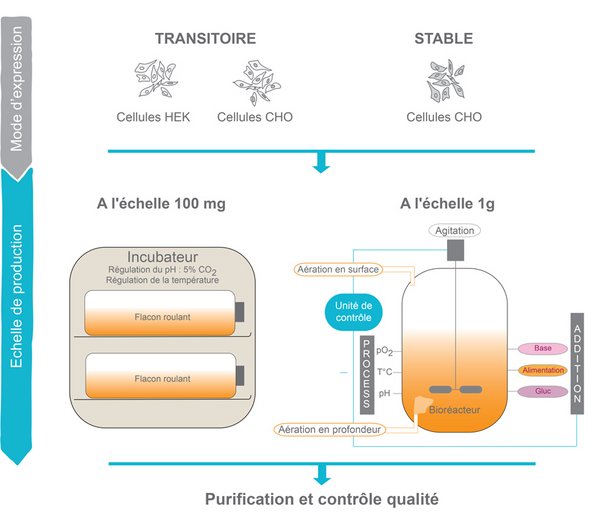
MImAbs produit aujourd’hui des anticorps jusqu’à l’échelle 100mg et ouvrira bientôt une unité de bioproduction à l’échelle du gramme. Les anticorps sont purifiés et contrôlés avant de les restituer à un client ou à l’unité d’immunopharmacologie pour des tests fonctionnels.
MImAbs propose deux modes d'expression d'anticorps :
• Expression transitoire dans des cellules HEK ou CHO pour une production ponctuelle et rapide (1 à 2 semaines). L'expression transitoire est généralement suffisante dans les premières étapes du développement d'un anticorps.
• Expression stable dans les lignées de cellules CHO, si des cycles de production répétés sont nécessaires. Ce système peut prendre jusqu'à 3 mois entre la transfection et la collecte, mais produit généralement de plus grandes quantités d'anticorps et est crucial une fois qu'un programme de développement d'anticorps est mature.
MImAbs travaille à des stades précoces vers une transition entre les systèmes d'expression transitoire et stable afin de garantir la développabilité des anticorps candidats.
MImAbs produit des anticorps de 1 mg à 400 mg ; l'échelle choisie dépend des applications prévues :
Les études in vitro nécessitent 1 à 2 mg d'anticorps. Les cellules sont cultivées dans des Cultiflasks de 25 ml et incubées dans un incubateur à agitation Sartorius Certomat CT. MImAbs peut produire jusqu'à 30 anticorps en parallèle à cette échelle en l'espace de 2 semaines.
Les études in vivo nécessitent jusqu'à 400 mg, pour lesquels les cellules sont cultivées en flacons rotatifs dans un volume allant jusqu'à 5 à 6 litres. En expression transitoire, 5 à 8 anticorps sont produits en parallèle à cette échelle en 8 semaines ; en expression stable, 2 anticorps sont produits en 12 jours.
MImAbs ouvrira bientôt une unité de bioproduction pour offrir une production d’anticorps à l’échelle du gramme.
Procédé de bioproduction standard dans les bioréacteurs

Contactez-nous pour plus d'information.
Les anticorps sont purifiés par chromatographie d’affinité. Ils sont formulés dans du PBS ou dans tout autre tampon, selon les besoins. Les anticorps sont caractérisés et contrôlés pour déterminer les paramètres suivants :
Paramètre | Technique | |
Concentration | Absorbance UV à 280nm | |
| Masse moléculaire | Spectrométrie de masse (Xevo G2S-QTof, Waters) | |
| Niveau de pureté des monomères | SEC-UPLC (UPLC Class Bio, Waters) | |
| Stabilité et formulation à long terme | Spectrométrie de masse (Xevo G2S-QTof, Waters) | |
SDS-PAGE | ||
| Niveau d’endotoxines | Test LAL de cinétique chromogénique |
Les résultats de ces analyses sont compilés dans un Certificat d’Analyse.
Détermination de la température de fusion (Tm) par la technique de Thermal Shift Assay (TSA) dans le tampon de formulation de l’anticorps (PBS 1X, pH 7,2 – 7,4)
Détermination de la stabilité thermique accélérée de l’anticorps par incubation à 40°C pendant 4 semaines, suivie d’une analyse SEC_UPLC
Une caractérisation précoce est réalisée sur des anticorps produits et purifiés à petite échelle :
Cible soluble : détermination du KD (Octet RED96, PALL ForteBIO)
Cible membranaire : détermination de l’EC50/ KD apparent (FACS)
Les tests fonctionnels sont ensuite effectués dans la plateforme de pharmacologie in vitro.