Les anticorps bi-spécifiques (Bi-Abs) capables de reconnaître et de diriger les cellules immunitaires pour détruire les cellules cancéreuses sont d’un intérêt particulier pour le développement de nouvelles immunothérapies. Le premier anticorps de ce type approuvé par la FDA est le blinatumomab, un bi-spécifique qui engage les lymphocytes T (via CD3ɛ humain) et qui est actuellement utilisé pour le traitement de la leucémie lymphoblastique aiguë à cellules B (CD19 humain exprimé à la surface).
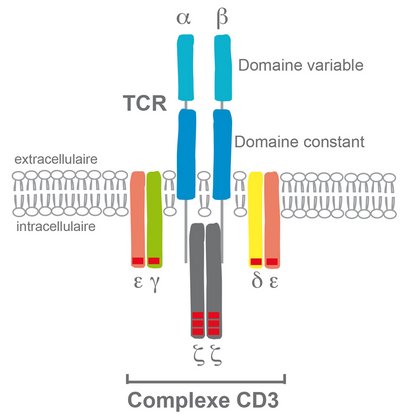
CD3ɛ est l’une des quatre sous-unités CD3 étroitement associées au récepteur TCR des cellules T :
L'une des principales limites du développement de Bi-Abs est la nécessité d'exprimer non pas une, mais deux protéines humaines chez la souris pour effectuer leur validation in vivo. MImAbs a entrepris le développement d’un modèle animal approprié pour la validation de tous les Bi-Abs dirigés contre CD3ε : une souris a été développée où le gène CD3ε murin a été humanisé. Ce modèle a été validé puisque des expériences in vitro et in vivo ont montré que ces souris ont un système immunitaire fonctionnel, en particulier des lymphocytes T fonctionnels, et constituent un modèle valable pour les Bi-Abs ciblant le CD3ε humain.
In Vitro: les cellules T de souris humanisées CD3ɛ sont correctement activées
Deux analyses ont été effectuées pour déterminer si les lymphocytes T exprimant le CD3ε humain, dérivés de la souris knock-in, étaient fonctionnels :
Test d’activation
Des lymphocytes T ont été isolés à partir de souris soit de type sauvage (WT), soit hétérozygotes (Het) ou homozygotes (Homo) pour hCD3ε. Ils ont subi un traitement avec un anti-CD28 soluble (1 µg / mL), en plus d’un anti-mCD3 (murin), ou un anti-hCD3 (humain), ou un anti-mTCRβ contrôle.
Le pourcentage de cellules T mCD8 + activées (CD69 + CD25 +) a été étudié par cytométrie en flux.
> Les cellules T de souris hCD3e homozygotes ou hétérozygotes sont bien activées avec l'anti-hCD3 + anti-CD28, et ce de manière dose-dépendante.
Test de cytotoxicité
Des cellules T effectrices de type sauvage (WT), hCD3ε hétérozygotes (Het) ou de hCD3ε homozygotes (Homo) ont été pré-activées avec un traitement anti-CD28 + anti-mTCRβ. Elles ont été incubées avec des cellules d’origine tumorale exprimant hCD19 et la luciférase (cellules Raji-Luc). La lyse cellulaire a été mesurée en présence de blinatumomab (bispécifique hCD19/hCD3ε).
> Les cellules T hCD3e homozygotes et hétérozygotes présentent une activité cytotoxique lorsqu'elles sont déclenchées via le récepteur hCD3e.
In vivo : activité anti-tumorale des bi-Abs ciblant le CD3ɛ humain
Pour tester l'effet antitumoral du blinatumomab in vivo dans le modèle humanisées CD3ɛ, les souris ont subi une injection par voie sous-cutanée de cellules murines de mélanome B16F10 transfectées pour exprimer hCD19, suivie d’un traitement intraveineux pendant 5 jours avec du Blinatumomab (hCD19-hCD3 bispécifique, 5 ou 20 μg / souris) ou un véhicule (lignes pointillées rouges ci-dessous). La survie des souris (A) et le volume de la tumeur (B) ont été surveillés. Les données démontrent une activité anti-tumorale modeste mais significative dans ce modèle. Cela peut être lié à l’activité modeste des bispécifiques contre les tumeurs solides chez l’homme, mais qui pourrait être améliorée par combinaison avec d’autres composés tels que des inhibiteurs de points de contrôle.